提供計画提出後の各種手続き
普段、再生医療を実施する中で、厚生局や再生医療等委員会に対して特にご連絡いただくことはございませんが、以下に掲げる場合につきましては、ご報告等お願いいたします。
- 一年ごとの定期報告をするとき 【定期】
- 提供計画の内容を変更するとき 【変更】【軽微変更】
- 提供計画を実施している中で、疾病等(疾病、障害若しくは死亡又は感染症)が発生したとき 【疾病等】
- 再生医療の提供を中止するとき 【中止】
1年ごとの定期報告 【定期】
再生医療等提供計画の受理日から1年ごとに、1年間の提供状況を報告書にまとめてください。作成した報告書は、まず再生医療等委員会に報告し、再生医療等委員会からの意見を聞いた上で各地方厚生局へお送りください。 当委員会にお送りいただく資料については 【一年ごとの定期報告】をご覧ください。 報告書の提出期限は、1年の満期を迎えてから90日以内です。
提供計画の内容を変更する時 【変更】【軽微変更】
再生医療等提供計画の内容を変更する場合、変更の手続きが必要です。
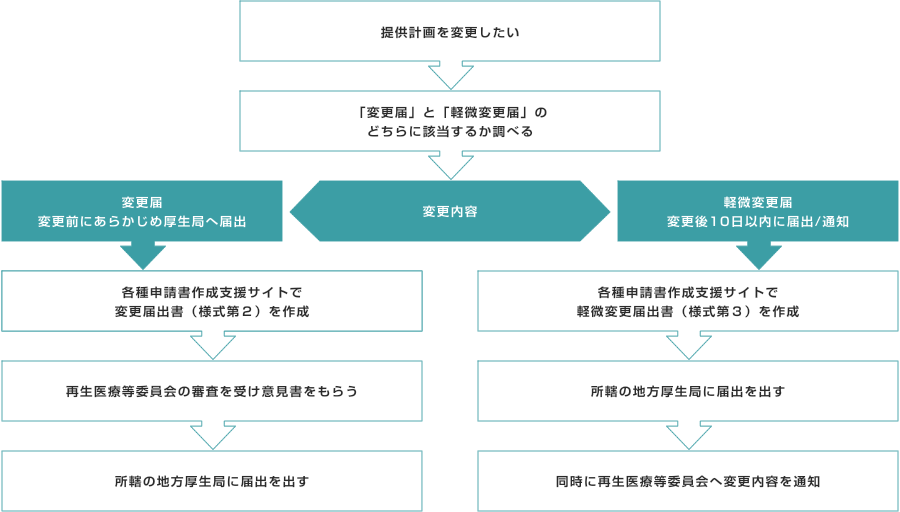
変更内容が軽微かどうか調べるには
変更内容が以下の選択肢に該当した場合「変更」、該当しなかった場合「軽微変更」となります。
- 当該再生医療等の安全性に影響を与える再生医療等の提供方法の変更
- 特定細胞加工物を用いる場合にあっては、当該再生医療等の安全性に影響を与える特定細胞加工物の製造及び品質管理の方法の変更
- 再生医療等製品を用いる場合にあっては、当該再生医療等製品に係る「用法、用量若しくは使用方法又は効能、効果若しくは性能に関する追加、変更又は削除」
- 再生医療等が研究として行われる場合にあっては、研究の実施方法の変更
- 前各号に掲げる変更のほか、当該再生医療等の安全性に影響を与えるもの
変更の審査を受ける場合
当委員会宛に審査で必要な資料と希望審査日時をお送りください。審査は対面、もしくはSKYPE等を用いたビデオ会議で行います。
当委員会にお送りいただく資料については各種申請書を作るには 【定期】【変更】【軽微変更】【疾病等】【中止】をご覧ください。
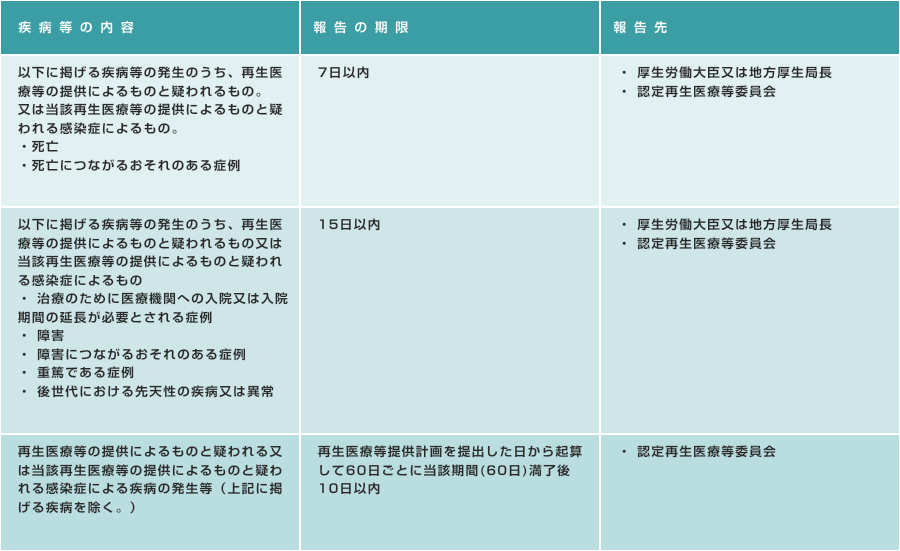
疾病等が発生した時 【疾病等】
再生医療等提供機関の管理者は、再生医療等提供計画に記載された再生医療等の提供に起因するものと疑われる疾病等の発生を知ったときは、以下のとおり報告してください。
当委員会にお送りいただく資料については各種申請書を作るには 【定期】【変更】【軽微変更】【疾病等】【中止】をご覧ください。
また、特定細胞加工物製造事業者又は再生医療等製品を用いた場合においては当該再生医療等製品の製造販売業者に対し、発生した事態及び講じた措置について速やかに通知してください。
再生医療等の提供を中止する時 【中止】
再生医療等提供計画に記載された再生医療等の提供を中止する場合、認定再生医療等委員会に通知するとともに、再生医療等提供中止届を提出してください。 当委員会にお送りいただく資料については各種申請書を作るには 【定期】【変更】【軽微変更】【疾病等】【中止】をご覧ください。 期限は、中止の日から10日以内です。
委員会にお送りいただく書類 【定期】【変更】【軽微変更】【疾病等】【中止】
当委員会へは下記の資料をお送りください。 「厚生局が出している様式」につきましては、「プレビュー版」もしくは「写し」をお送りください。
 申込書(変更・疾病等・定期)のダウンロード
申込書(変更・疾病等・定期)のダウンロード※プレビュー版の作り方は下図をご参照ください。
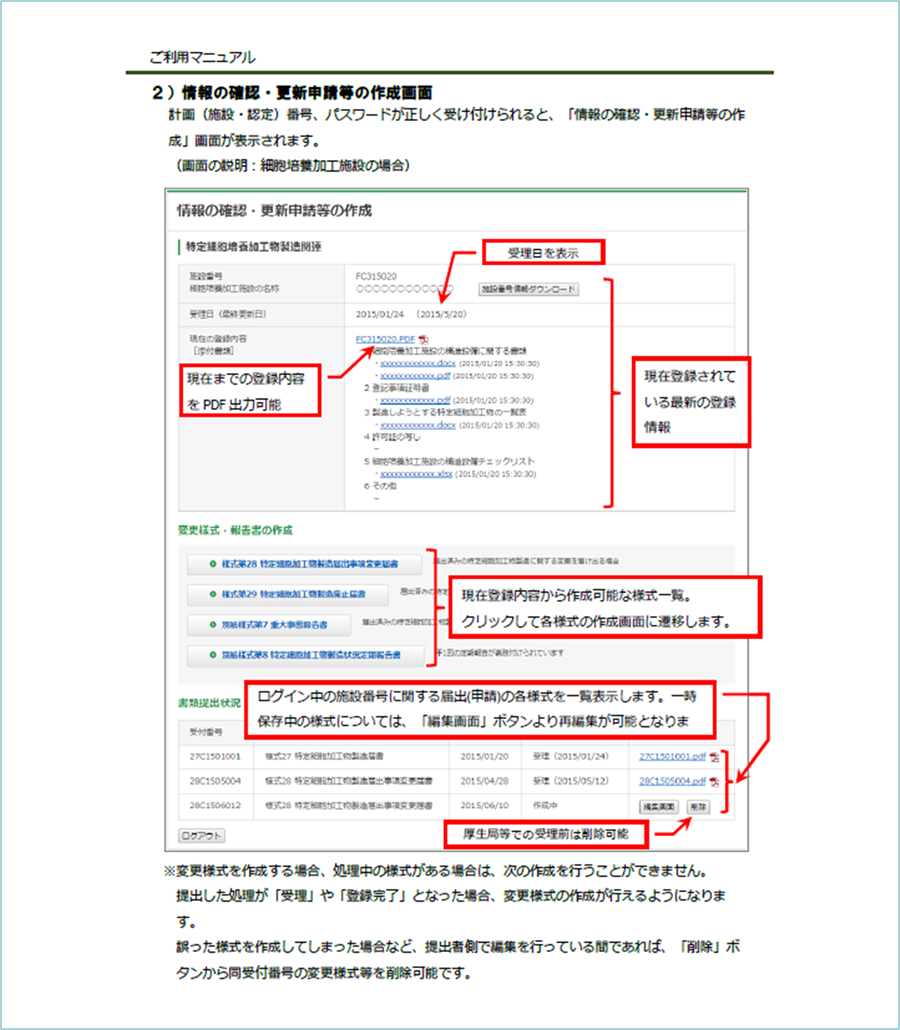
 (再生医療等の安全性の確保等に関する法律 「各種申請書作成支援サイト」ご利用マニュアルより)
(再生医療等の安全性の確保等に関する法律 「各種申請書作成支援サイト」ご利用マニュアルより)
各種申請書を作るには 【定期】【変更】【軽微変更】【疾病等】【中止】
各種申請書作成支援サイトからログインして各種書類を作成してください。
http://saiseiiryo.mhlw.go.jp/application/plan
各種申請書作成支援サイトの使い方が分からない場合、以下のページから操作マニュアルをダウンロードし、「変更等申請・届出、報告書の作成」の項を参照なさってください。
http://saiseiiryo.mhlw.go.jp/pages/about/
マニュアルサンプル(P19,P20)