- 提供計画の審査依頼
- 提供計画受理後の申請
- 一年ごとの定期報告
審査のご依頼
- 当委員会は第三種のみの提供計画を審査する認定委員会となります。第一種・第二種の提供計画の内容については意見書をお出しすることができません。
- 再生医療に使用する細胞を培養・加工するためには、製造施設ごとに事前に届出等をしておく必要があります。当委員会の審査は、施設の届出等が終わった後に行うものになります。
- 提供計画の作成には、メールアドレスが必要です。メールアドレスをお持ちでない場合は、審査のお申込み前に取得してください。
- 当委員会では再生医療等提供基準チェックリストを基準に審査を致しますので、提供計画を提出される先生方が審査を受ける際には当該基準を十分にご理解の上、参加していただきます様お願い申し上げます。
審査の結果、再生医療等提供基準に適合していないと判断される場合には、追加の審査を後日開催させていただきます。
基準に適合しない場合には意見書の発行ができないこともございます。 - 審査は原則として東京都内で行います。遠方の方はご相談ください。
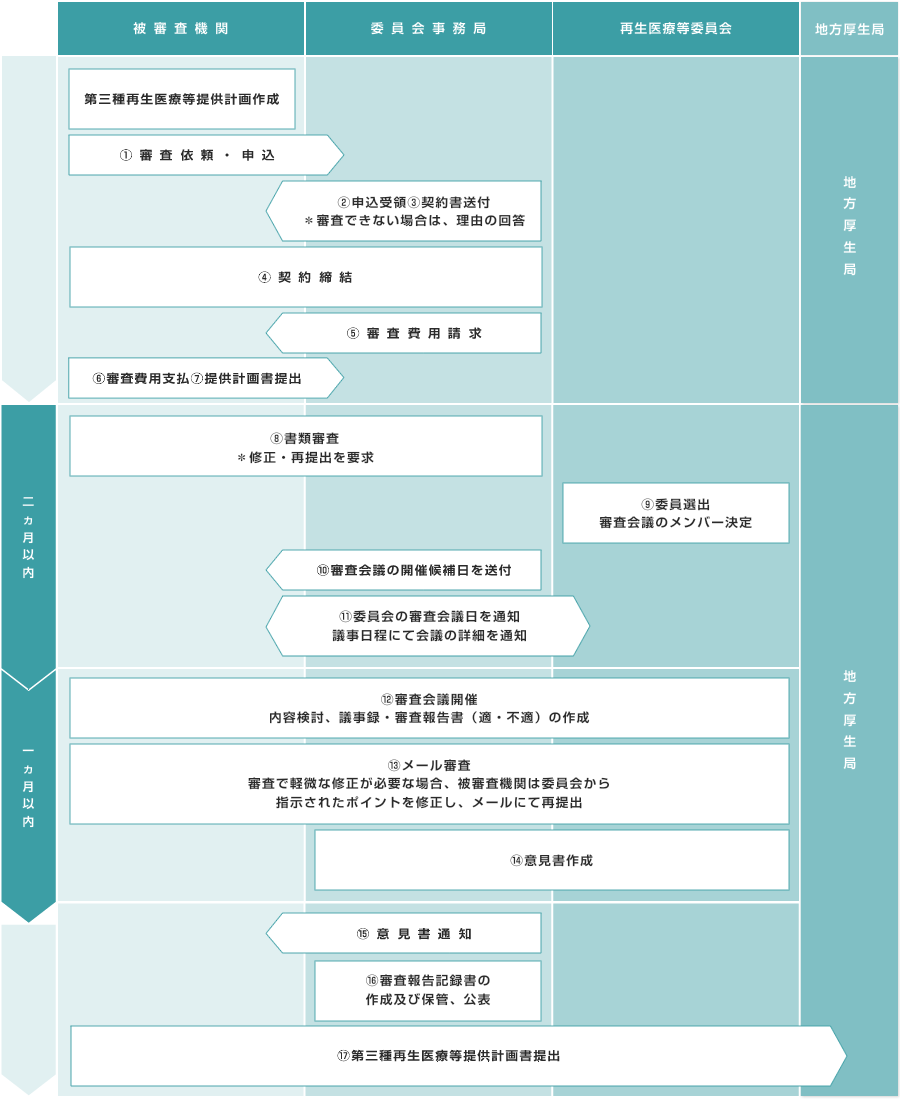
審査ご依頼から意見書の発行までの流れ
再生医療等委員会スケジュール
日本薬事法務学会再生医療等委員会は月2回、年24回の定例開催を予定しております。
- 令和2年3月30日(月)9:00~11:00
- 令和2年3月16日 申込締切
- 令和2年4月10日(金)9:00~11:00
- 令和2年3月27日 申込締切
- 令和2年4月20日(月)9:00~11:00
- 令和2年4月6日 申込締切
申込み
受付締切日の17時までに、審査申込時に必要な資料を添付の上、メールをお送りください。 メールアドレスは申込書に記載しております。審査申込時に必要な書類
- 1
- 様式第1 再生医療等提供計画
- 2
- (様式第1 再生医療等提供計画の添付書類)
2-1.提供する再生医療等の詳細を記した書類
2-2.実施責任者及び再生医療等を行う医師又は歯科医師の氏名、所属、役職及び略歴(研究に関する実績がある場合には、当該実績を含む。)を記載した書類
2-3.再生医療等に用いる細胞の提供を受ける場合にあっては、細胞提供者又は代諾者に対する説明文書及び同意文書の様式(細胞の提供を受ける場合)
2-4.再生医療等を受ける者に対する説明文書及び同意文書の様式
2-5.再生医療等提供計画に記載された再生医療等と同種又は類似の再生医療等に関する国内外の実施状況を記載した書類
2-6.再生医療等に用いる細胞に関連する研究を記載した書類
2-7.特定細胞加工物概要書、特定細胞加工物標準書、衛生管理基準書、製造管理基準書及び品質管理基準書(特定細胞加工物を用いる場合)
2-8.再生医療等製品の添付文書等(再生医療等製品を用いる場合)
2-9.再生医療等の内容をできる限り平易な表現を用いて記載したもの
2-10.委託契約書の写しその他これに準ずるもの(特定細胞加工物の製造を委託する場合)
2-11.個人情報取扱実施規程
2-12.手順書
2-13.再生医療等提供計画の情報の公表に関する同意書
2-14.その他本文中に掲載しきれない説明書類等 - 3
- 再生医療等提供基準チェックリスト(様式第1と添付書類の内容を確認)
- 4
- 第三種再生医療等提供計画審査申込書


